zurück zu Kapitel III
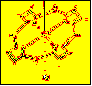
- 1. Struktur des Hämoglobins
- 2. HB-Bestimmung mittels Hämiglobin-Methode (Praktikumsbeispiel)
- 3. Durchschnittswerte für die[Hb] und Abweichungen
- 4. Zur Pufferfunktion des Hb
- 5. O2-Anlagerung und O2-Transport im Blut
- 6. O2-Bindungskurve; O2-Sättigung
- 7. Ursachen für die Verschiebung der O2-Bindungskurve
- 8. Abhängigkeit der O2-Bindungskurven vom CO2-Partialdruck
- 9. O2-Bindungskurve des fetalen Blutes
- 10. Hypoxie, Anoxie
- 11. Zwischenfragen
1. Struktur des Hämoglobins
Hämogobin (Bb) transportiert O2 als Oxyhämoglobin (HbO2) von der Lunge zu den Organen und einen Teil des CO2 wieder zurück aus den Geweben und Organen zur Lunge.
Das Chromoprotein enthälte 4 Polypeptidketten (Hb A [A von Adult], zwei a-Ketten mit je 141 AS und zwei b-Ketten à 146 AS; bei Sichelzellanämie ist dabei an der 6. Stelle statt Glu Val zu finden; das fetale Hb weist statt den b-Ketten g-Ketten auf; es sind insgesamt über 200 Hb-Arten mit definiertem AS-Austausch bekannt, wobei die Symptome meist unauffällig bleiben; die monomeren Ketten des Myoglobins sind übrigens den Hb-Ketten homolog) und als prosthetische Gruppe je ein Häm.
Markante Stellen der Hämsynthese: Succinyl-CoA (aus dem Citratcyclus) + Glycin (Chemin Weg) ® 5-Aminolävulinsäure mal 2 ® Porphobilinogen ® Protporphyrin ® Einbau von teilweise wiedergewonnenem Eisen (Ammenzellen) ® Häm.
Das Grundgerüst wird alsodurch 4 Pyrrolringe dargestellt, die je eine Methyl- und eine Vinyl- bzw. Propionsäure-Seitenkelle tragen. Im D-Ring sind die sonst regelmäßig angeordneten Seitenketten umgekehrt. Die vier Pyrrolringe sind über Methingruppen verbunden (Farbcharakter durch Delokalisierunjg der p-Elektronen).
Durch das zweiwertige zentrale Eisen (Fe++) wird aus dem Protoporphyrin das Häm. Koordinationsstellen des Eisens sind dabei durch den Porphyrinring besetzt (2 Haupt- und 2 Nebenvalenzen), eine wird von einem Histidin-Rest des Proteins in Anspruch genommen und die 6. Koordinationsstelle kann O2 reversibel anlagern (Man nennt Hb auch “Enzym honoris causa”, weil die reversible “O2-Bindung”, bzw. lockere Anlagerung, der Bindung eines Substrates an ein Enzym gleicht). Durch die O2-Anlagerung wird die Wertigkeit des Fe++ nicht geändert (daher auch die Bezeichnung Oxygenation für die Anlagerung und Desoxygenation für die Abgabe von O2 und nicht Oxydation und Reduktion). Falls richtig oxydiert wird, entsteht Methämoglobin (Hämiglobin) mit einem Fe3+, welches nicht mehr zum O2-Transport befähigt ist. Hämi globin kommt normal aber nie in geringen Mengen vor, weil Flutathion im Ery. das Hb einerseits vor Oxydation schützt und andererseits Hämiglobin wieder zu Hb reduzieren kann.
